Zadanie
Potom, ako Kubo nakúpil bufet, rozhodol sa, že umyje aj to nekonečne špinavé denko1. Pochopiteľne, takú riadne špinavú doštičku treba nechať odmočiť. Vtom si Kubo uvedomil, že ak napustí umývadlo čistou vodou, nevzniknú mu bubliny, ktoré má tak rád. Kubovi preleteli hlavou otázky:
- „Prečo nedokážem nafúknuť bublinu z čistej vody?“
- „Čo robí mydlo, že z mydlovej viem?“
- „Prečo to funguje?“
Keďže Kubo je na matfyze ešte iba prvák, obracia sa s týmito otázkami na vás.
doska na krájanie↩︎
Na začiatok by sme Kuba radi upozornili, že nie je pravda, že by bubliny z vody vôbec neexistovali. Skúste si napríklad napustiť vodou nejakú nádobu. Počas celého tohto procesu je možné takéto bublinky na hladine pozorovať (obr. bublinky ). Problém je však v tom, že zaniknú veľmi rýchlo. Keď zopakujeme tento experiment s mydlovou vodou, bublinky vydržia neporovnateľne dlhšie.
Proti existencii bubliniek z vody by sme ale stále mohli argumentovať tým, že za uspokojujúcu bublinu z vody považujeme len takú vznášajúcu sa vo vzduchu. Takú pravdepodobne nikto z vás nikdy nepozoroval. Ale naozaj také neexistujú? Popravde, astronauti to šťastie pozorovať ich mali – dúfam, že ako dôkaz postačí toto alebo toto video. Poďme sa pozrieť, aká sa za bublinkami skrýva fyzika a následne sa pokúsiť tieto pozorovania vysvetliť.

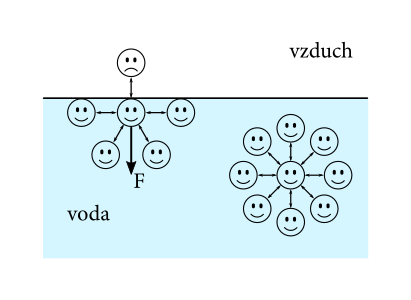
Začnime vysvetlením fyzikálneho javu zvaného povrchové napätie. Molekuly vody sa navzájom priťahujú medzimolekulovými silami. Výslednica týchto síl na molekulu vo vnútri kvapaliny je nulová, pretože sila od molekúl je zo všetkých smerov rovnaká. Ak sa ale molekula nachádza na povrchu, výslednica všetkých síl už nulová nie je. Molekuly vzduchu sa totiž majú s molekulami vody menej radi než molekuly vody navzájom a preto výslednica medzimolekulových síl pôsobiacich na molekulu na povrchu bude kolmá na povrch kvapaliny, a orientovaná smerom do vnútra (viď obrázok sily ).
Na premiestnenie molekúl do povrchovej vrstvy je teda potrebné vykonať prácu, a teda molekulám na povrchu prislúcha aj väčšia energia. Celkovo sa ukáže, že prírastok energie za tieto molekuly na povrchu – povrchová energia – bude priamo úmerný ploche \(S\): \(E = \sigma \cdot S\), kde konštanta úmernosti \(\sigma\) (čo je v tomto prípade aj plošná hustota energie) je charakterizovaná tým, aké látky tento povrch oddeľuje a nazýva sa povrchové napätie (napr. pre vodu v styku so vzduchom pri \(\SI{20}{\celsius}\) je \(\sigma_{\mathrm{H_2O}} = \SI{0.072}{\newton\per\metre}\), pre mydlovú vodu v styku so vzduchom to zvykne byť zhruba \(\sigma_{\mathrm{H_2O}}/3\)). Snaha minimalizovať energiu prirodzene spôsobuje, že povrchová vrstva sa správa ako pružná blana snažiaca sa stiahnuť na plochu s najmenším obsahom. Povrchové napätie je teda tiež dobrou mierou kontraktívnej tendencie kvapalín umožňujúcej odporovať deformáciám spôsobeným vplyvom vonkajších síl.
Môže byť ale fakt, že na zemi pozorujeme bublinky z mydlovej vody ale nie z čistej vody, spôsobený čisto tým, že bublinke s rovnakým povrchom z čistej vody prináleží približne trikrát väčšia povrchová energia? Koncept s povrchovou energiou sa v nulovej gravitácii nezmení a vodové bubliny tam pozorovať vieme a vyzerajú aj celkom stabilne. Samozrejme, bublina nie je stavom s najmenšou energiou, ale to nie je ani v prípade mydlovej vody. Vždy sa viac oplatí kvapka. Netvrdíme, že mať menšiu energiu nie je výhodou, ale keďže takéto zdôvodnenie nie je samo o sebe presvedčivé a je ťažké ho dokázať, poďme sa pozrieť, či pes nie je zakopaný aj v niečom inom.
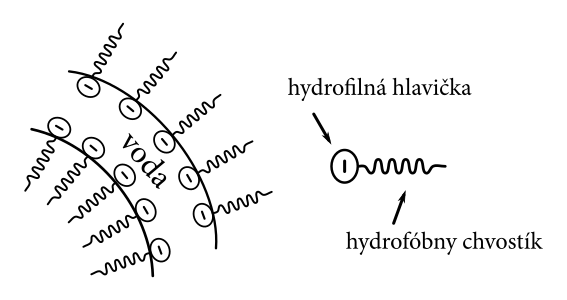
Čím iným je mydlo ešte špeciálne? Svojou štruktúrou. Molekuly mydla, ako to už u tenzidov (angl. surfactant) býva, sa skladajú z 2 častí – hydrofilnej hlavičky, ktorá má rada vodu, a hydrofóbneho chvostíka, ktorý chce byť od vody čo najďalej. Je teda prirodzené, že týmto molekulám sa po pridaní do vody bude na povrchu páčiť (chvostíky sa tam vyhnú kontaktu s vodou). Efektívne sa teda v prípade bubliny vytvorí vrstvenie mydlo-voda-mydlo (viď obr. tenzid ), ktoré jednak chráni bublinu pred rýchlym vyparovaním a stenčovaním vonkajšej vrstvy a dvak zníži povrchové napätie a tým aj energiu, vďaka tomu, že molekuly mydla prebýjajúce sa na povrch odseparujú molekuly vody navzájom a vzdialenejšie molekuly vody sa priťahujú slabšími silami.1
Veľmi dôležitý vplyv má aj Marangoniho efekt. Marangoniho efekt nastáva, keď sa na hladine kvapaliny vyskytnú dve oblasti s rozdielnym povrchovým napätím (napríklad keď sa na dve miestach bude líšiť koncentrácia (percentuálne množstvo) mydlových molekúl). Keďže v oblasti s vyšším povrchovým napätím pôsobia vyššie kontraktívne sily, molekuly na rozhraní týchto oblastí budú silnejšie ťahané do časti s vyšším povrchovým napätím.
Ak teda napríklad do pohára s vodou kvapneme kvapku mydla, mydlo lokálne zníži povrchové napätie a preto sa vytvorí prúd molekúl, ktorý smeruje smerom od časti kvapaliny s nižšou hodnotou povrchového napätia (miesto s mydlom) do časti s vyššou hodnotou povrchového napätia. Takýto proces sa deje, kým sa povrchové napätie na kvapaline nevyrovná, a teda kým molekuly mydla nie sú rozmiestnené rovnomerne po celej hladine.
Názornú ukážku, ako sa spolu s molekulami vody v smere tohto nárastu pohybujú častice čierneho korenia si môžete pozrieť napríklad tu. Aká je užitočnosť tohto javu pre mydlovú bublinu? Keď sa povrchová vrstva natiahne, povrchová koncetrácia mydlových molekúl poklesne, čím narastie povrchové napätie. Mydlo teda selektívne posilňuje najslabšie časti bubliny a bráni ich výraznejšiemu naťahovaniu.
V čom sú teda mydlové bubliny špeciálne? Stoja nás menej energie, pomalšie sa odparujú a vďaka Marangoniho efektu posilňujú svoje najslabšie časti. A ako môžete pozorovať napríklad tu, mydlové bubliny sú vo výsledku aj celkom odolné.
Priznávame, že toto vysvetlenie je silne odmávané rukami. Je veľmi ťažké prediskutovať, aké presne rozloženie mydlových molekúl a molekúl vody pri povrchu bude a aké sily medzi nimi navzájom pôsobia. Molekuly mydla sa budú pravdepodobne navzájom trochu odpudzovať, keďže ich hlavičky majú vo vode negatívny náboj, ale vďaka nemu sa pravdepodobne zvládnu viazať vodíkovými mostíkmi na molekuly vody. V každom prípade, ako experimentálne pozorujeme, celková sila ťahajúca molekulu na povrchu do vnútra sa zníži zhruba na tretinu.↩︎
Diskusia
Tu môžte voľne diskutovať o riešení, deliť sa o svoje kusy kódu a podobne.
Pre pridávanie komentárov sa musíš prihlásiť.